Содержание
Борьба с полиомиелитом — это пример победы вакцин над одной из самых страшных инфекций, известных человечеству. К сожалению, эту победу пока нельзя считать окончательной. В новой статье спецпроекта «Вакцинация» мы расскажем, почему дети до сих пор иногда болеют полиомиелитом, зачем вакцинировать там, где болезни давно нет, и как это делать правильно.

Вакцинация

Генеральный партнер спецпроекта — Фонд Зимина.
Изобретение вакцин коренным образом изменило жизнь человечества. Многие заболевания, которые ежегодно уносили тысячи, если не миллионы жизней, в настоящее время практически не существуют. В данном конкретном проекте мы не только рассказываем об истории вакцин, общих принципах их разработки и роли вакцинопрофилактики в современном здравоохранении (этому посвящены первые три статьи), но и подробно рассказываем о каждой вакцине включенных в Национальный календарь прививок, а также вакцин против гриппа и вируса папилломы человека. Вы узнаете о том, что собой представляет каждый из возбудителей, какие варианты вакцин существуют и чем они отличаются друг от друга, затронем тему поствакцинальных осложнений и эффективности вакцин.
Для сохранения объективности кураторами спецпроекта мы пригласили Александра Соломоновича Апта, доктора биологических наук, профессора МГУ, заведующего лабораторией иммуногенетики НИИ туберкулеза (Москва); , — а также Сергей Александрович Бутрия — педиатр, автор блога «Записки педиатра».
Полиомиелит — удивительно известная болезнь, учитывая, что сегодня она встречается крайне редко. В 2019 году во всем мире было зарегистрировано всего 176 случаев дикого вируса.
Но так было не всегда. Эпидемии полиомиелита, начавшиеся в середине ХХ века, не могли быть остановлены надолго. Вакцины против инфекции были разработаны не сразу: понадобились годы, в течение которых тысячи детей умерли, а десятки тысяч стали инвалидами. В довакцинальную эпоху заболеваемость полиомиелитом составляла примерно 600 000 случаев в год. В 1988 году, когда была создана Глобальная инициатива по борьбе с полиомиелитом, ежегодно инфекцией заражалось 350 000 детей во всем мире. Само заболевание до сих пор практически неизлечимо (рис. 1). Сегодня в мире насчитывается около 20 миллионов жертв полиомиелита 1.
В статье «История вакцинации» [20] нашего спецпроекта отдельная глава посвящена поворотному моменту в борьбе с полиомиелитом — разработке первой вакцины против полиомиелита. — Эд.
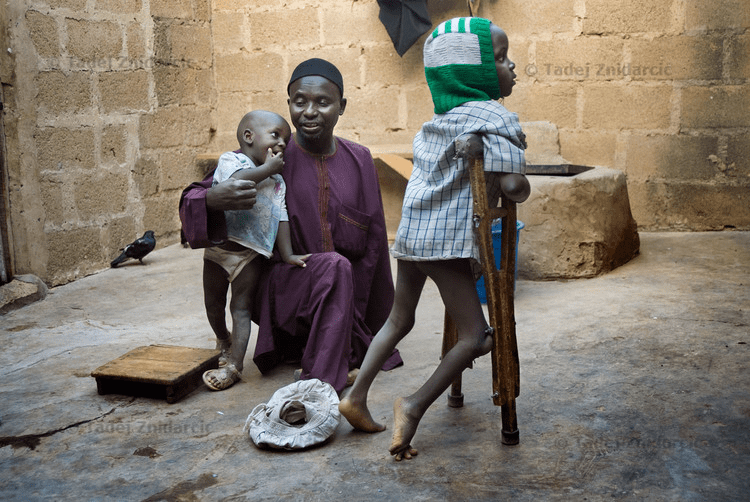
Рисунок 1а. Жертвы полиомиелита в Нигерии, где до сих пор циркулирует дикий вирус полиомиелита. Умар, переживший полиомиелит, родился в 2003 году, когда в нигерийском штате Кано бойкотировали детские прививки. Мальчик ходит на костылях.
Жизнь с полиомиелитом в Северной Нигерии
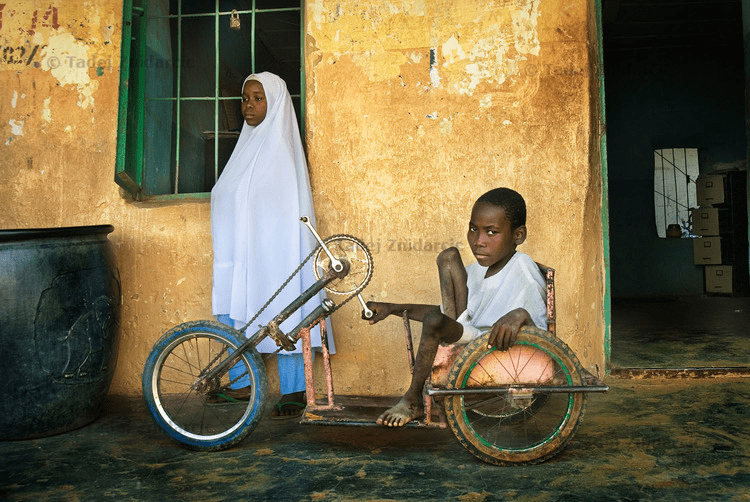
Рисунок 1б. Жертвы полиомиелита в Нигерии, где до сих пор циркулирует дикий вирус полиомиелита. Наджа Ату Юсиф (слева) после выздоровления от полиомиелита стал хромать. Ее брат Адаму Юсиф не может ходить из-за болезни и передвигается на трехколесном велосипеде.
Жизнь с полиомиелитом в Северной Нигерии
Полиомиелит — болезнь грязных рук
Полиомиелит в основном детская болезнь. В развивающихся странах 65–75% случаев инфицирования приходится на детей в возрасте до 3 лет и 95% — на детей в возрасте до 5 лет. Маленькие дети более восприимчивы к инфекции, так как полиомиелит передается через грязные игрушки и посуду. Молодым и взрослым тоже есть чего опасаться – у них осложнения после заражения более серьезные и встречаются чаще. Смертность от полиомиелита у детей составляет 5%, у взрослых – 15–30% [2].
Изучение останков мумий и старых снимков дает понять, что полиомиелит был с нами очень давно. Был распространен в Древнем Риме, Греции и Египте (рис. 2).

Рисунок 2а. Полиомиелит в древности: обложка документа ВОЗ, объявляющего ЕС регионом, свободным от полиомиелита, 2002 г. На изображении изображена надгробная плита 18-й египетской династии (580–1350 гг до н.э.). Изображенный на ней человек переболел полиомиелитом и остался инвалидом. Правая нога повреждена из-за болезни.
«Сертификация ликвидации полиомиелита»

Рисунок 2б. Полиомиелит в древности: сосуд из захоронения в Италии (480 г до н.э.). Бог старости Гера изображен на рисунке с деформированным позвоночником и атрофированными мышцами — характерными признаками полиомиелита.
Полиомиелит в Древней Греции (5 век до н.э)?
Ученые всего мира изучают полиомиелит с конца 19 века, до этого о нем почти ничего не было известно (рис. 3).

Рисунок 3. История изучения полиомиелита. 1840 г. — немецкий ортопед Якоб Гейне выделил полиомиелит в отдельное заболевание, назвав его детским спинальным параличом. 1890 — Шведский педиатр Карл Оскар Медин доказал заразную природу болезни. 1909 г. — Полиовирус был впервые выделен в Австрии Карлом Ландштейнером и Эрвином Поппером. 1913 г. — румынский бактериолог Константин Левадити культивировал полиовирус на живых клетках. 1931 г. — сэр Фрэнк Макфарлейн Бернет и Джин Макнамара в Австралии открыли три серотипа полиовируса. 1938 г. — Американский врач и вирусолог Альберт Сабин доказал, что основными портами заражения являются ротовая полость и другие отделы пищеварительного тракта. 1949 — В США Джон Эндерс и его коллеги разработали метод выращивания полиовируса в культуре клеток почек обезьян. Исследователи получили Нобелевскую премию за свою работу. 1950 — В США Джеральд Кокс и Хилари Копровски получили первую версию живой вакцины на основе штаммов, ослабленных пассажем через мозг хлопковых крыс. 1955 – американец Джонас Солк создал первую в мире инактивированную вакцину против полиомиелита. 1956 г. — Альберт Сабин получил ослабленные штаммы полиовируса, которые были использованы для создания живой пероральной вакцины. 1959 г. — российские ученые Михаил Чумаков и Анатолий Смородинцев создали и внедрили живую полиомиелитную вакцину в виде сиропа или драже на основе штаммов Сэбина. 1981 — Геном полиовируса был расшифрован двумя независимыми группами исследователей. 2015 г. — ликвидирован дикий полиовирус типа 2. Последний раз случай вызванного им полиомиелита был зафиксирован в 1999 году. 2019 год — ликвидирован дикий полиовирус 3 типа. Диагноз не ставится с 2012 года.
иллюстрация Ирины Ефремовой
Другое название полиомиелита — болезнь Гейне-Медина. Речь идет о двух врачах, которые начали борьбу с инфекцией. Якоб Гейне в 1840 г в Германии отличил полиомиелит от других видов паралича, а Карл Медин из Швеции через 50 лет доказал его заразную природу и показал, что не все случаи полиомиелита заканчиваются поражением нервной системы.
Крошка-вирус
Полиовирус хорошо изучен. Он относится к роду энтеровирусов (тип — энтеровирус С), обитающих в пищеварительном тракте, к семейству пикорнавирусов — мелких вирусов (piccolo — «маленький» по-итальянски) с геномом в виде молекулы РНК. Пикорнавирусы отличаются простой структурой: одноцепочечная (+) РНК (положительная или кодирующая) и окружающая ее белковая оболочка — капсид (рис. 4).
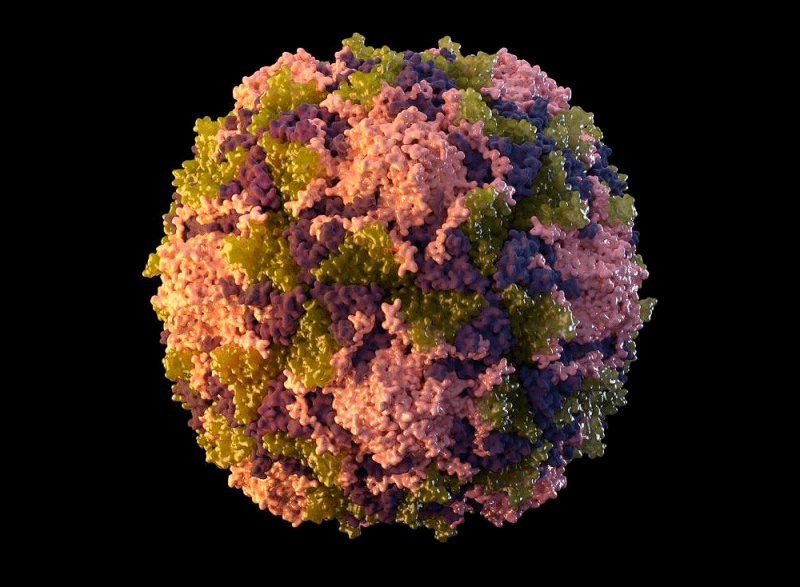
Рисунок 4а. 3D-модель вируса полиомиелита
[восемь]
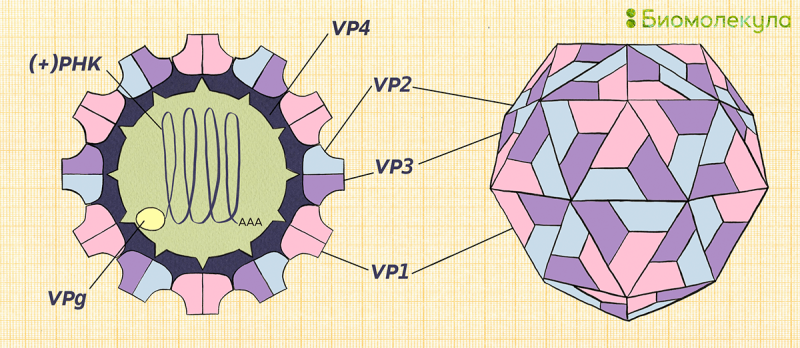
Рисунок 4б. Структурная схема полиовируса. Полиовирус имеет небольшие размеры – это частицы диаметром около 30 нм. Он имеет шестиугольную форму, хотя на микрофотографиях может показаться круглым, и состоит из белкового капсида и одноцепочечной геномной (+) РНК размером примерно 7,5 т.п.н. 5′-конец генома связан с белком VPg. Капсидные белки включают три внешних (VP1, VP2 и VP3) и один внутренний (VP4).
иллюстрация Ирины Ефремовой
Дикие полиовирусы делятся на три серотипа (1, 2 и 3) в зависимости от конфигурации белков на их поверхности. Все серотипы вызывают полиомиелит у человека, и иммунитет к одному типу вируса не защищает от других.
Белковая оболочка вируса надежно защищает его от внешних воздействий. Полиовирус может жить в воде несколько месяцев, а в среде, богатой органическими веществами (например, фекалиях) — до полугода. Чтобы оправдать название энтеровируса, он устойчив к кислой среде желудочно-кишечного тракта. Капсид полиовируса не содержит липидов, и поэтому даже обработка спиртом или хлороформом, растворяющим жир, ему бесполезна. Полиовирус без проблем переживает холод, но быстро инактивируется при температуре выше 50°С. Геном вируса полиомиелита кодирует один крупный белок-предшественник, из которого вырезаны все белки, необходимые вирусу (рис. 5).
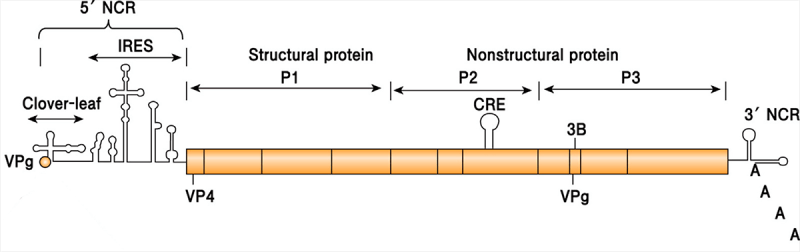
Рисунок 5. Организация генома полиовируса. Вирусная (+) РНК кодирует один большой белок-предшественник, который затем расщепляется на четыре структурных (районы P1) и несколько неструктурных (районы P2 и P3) белков. 5′-конец генома связан с белком VPg (белок вириона, связанный с геномом), а 3′-конец имеет поли(А)-хвост. Без него РНК полиовируса теряет свою инфекционность. На обоих концах РНК также есть некодирующие области (NCR). 5′-NCR включает сайты для репликации и трансляции РНК. 3′-NCR необходим для инициации синтеза (-) РНК (отрицательный). CRE (цис-действующий элемент репликации) представляет собой цис-действующий элемент репликации, необходимый для репликации (+) РНК.
[3]
Полиовирус проникает в клетки человека путем присоединения к расположенному на них гликопротеину CD155, который проникает через клеточную мембрану и обнажает три ее домена (рис. 6). Из-за этого CD155 был назван «рецептором полиовируса» или PVR (рецептор полиовируса человека). Клетки нуждаются в ПВР для собственных нужд (например, для клеточной адгезии), но вирус использует его в своих целях, а именно для проникновения в клетки и их подавления.
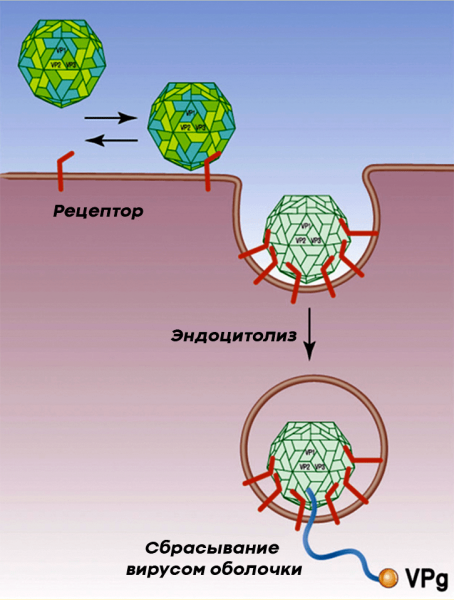
Рисунок 6. Полиовирус прикрепляется к PVR нервной клетки и проникает через эндоцитоз. Медиатором проникновения полиовируса в клетку является гликопротеин CD155.
иллюстрация Ирины Ефремовой по [3]
PVR — не просто рецептор
Рецептор полиовируса человека (PVR) представляет собой белок на поверхности наших клеток, выполняющий множество различных функций. Он обеспечивает правильную адгезию клеток, участвует в движении и пролиферации (размножении) клеток, особенно в период эмбрионального развития. PVR также известен как регулятор клеточного иммунитета. Он помогает лейкоцитам проходить через стенки сосудов, продвигаясь к очагу воспаления.
Интересно, что PVR присутствует в большом количестве на поверхности опухолевых клеток (эпидермальный и остеогенный рак, рак молочной железы и толстой кишки, нейробластома и др.) благодаря постоянной активности морфогенного фактора Sonic hedgehog и транскрипционных факторов Gli1 и Gli3 [4].. Во всех здоровых клетках PVR экспрессируется на низком уровне, что делает его отличным маркером различных типов опухолей.
Исследователи используют PVR на поверхности опухолевых клеток для борьбы с раком. В качестве противоопухолевых препаратов они предлагают генетически модифицированные безопасные полиовирусы, разрушающие опухоль, но не поражающие соседние ткани [5], [6].
После проникновения в цитоплазму клетки-хозяина полиовирус начинает размножаться (рис. 7). Для этого он должен скопировать собственную РНК, но сначала восполнить вирусные структурные и неструктурные белки. Последние необходимы вирусу для копирования собственного генома. Новые вирионы образуются из копий вирусной РНК и структурных белков в инфицированных клетках. Цикл репродукции вируса в клетке занимает всего семь часов.
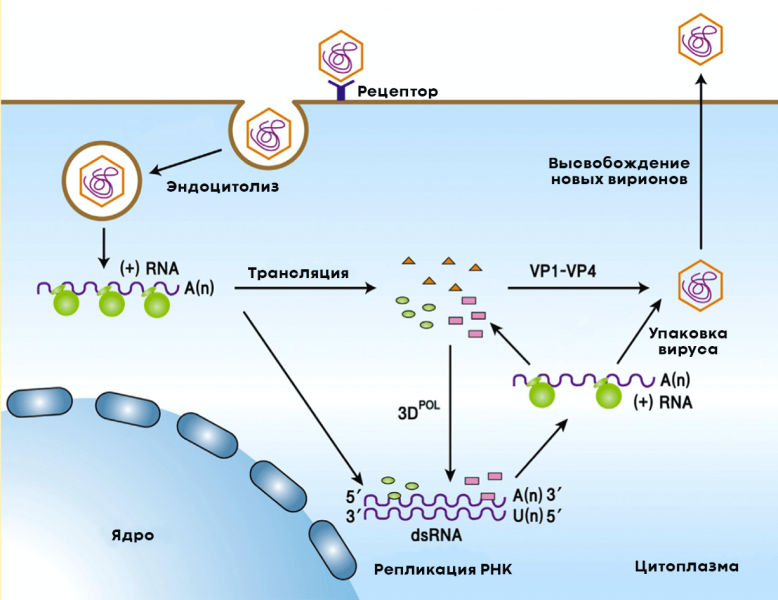
Рисунок 7. Жизненный цикл полиовируса в клетках человека. Вирус проникает в клетку путем эндоцитоза и взаимодействует с рецептором CD155. При этом изменяется конформация структурных белков вириона, и вирусная (+) РНК попадает в цитоплазму, где начинает копировать вирус. На первом этапе в качестве мРНК для трансляции белка используется геномная (+)РНК, после чего начинается репликация геномной (+)РНК с образованием промежуточной (-)РНК. Синтезированные (+)РНК упаковываются в капсиды, состоящие из структурных вирусных белков, образуя новые вирионы. Клетка разрушается, вирус выходит наружу.
иллюстрация Ирины Ефремовой по [3]
Полиомиелитная рулетка
Полиомиелит имеет два пути передачи. В развивающихся странах заражение полиомиелитом происходит в основном через зараженную пищу и воду, куда полиовирус попадает с фекалиями больных, а в регионах с высоким уровнем гигиены заражение происходит через капельки слюны при кашле, чихании или разговоре на первый план.
Человек начинает выделять полиовирус через 2–4 дня после заражения. В носоглотке он сохраняется в течение 1–2 недель [7]. Одной из причин такой резистентности полиовируса является его способность сохраняться в желудочно-кишечном тракте в течение длительного времени и выделяться в окружающую среду в течение недель или месяцев. Учитывая, что инфекция может протекать бессимптомно, становится понятно, что уберечь ребенка от заражения полиомиелитом очень сложно.
При попадании в наш организм через рот вирус проникает на слизистую оболочку верхних дыхательных путей и желудочно-кишечного тракта и начинает активно размножаться в носоглотке (в аденоидах и миндалинах) и тонком кишечнике (в лимфатических узлах — пейеровых бляшках).). Инкубационный период заболевания колеблется от 3 до 35 дней, в среднем 7–10 дней.
Существует несколько сценариев дальнейшего развития инфекции.
Около 72% людей, заразившихся вирусом, не ощущают никаких симптомов, полиомиелит проходит для них незаметно. Есть и такие (около 24%), у которых после окончания инкубационного периода в течение нескольких дней наблюдается лихорадка, расстройство желудка, боль в горле, тошнота, головная боль и утомляемость. Но в остальных случаях полиомиелит так просто не сдается [8].
Довольно редко, примерно у 4% инфицированных, вследствие полиовируса возникает асептический менингит — воспаление мозговых оболочек. Тяжело переносится, сопровождается лихорадкой, сильной головной болью и рвотой, но обычно заканчивается выздоровлением.
Наконец, примерно в одном из 200 случаев вирус перемещается с лимфой и кровью к нервным волокнам и проникает в моторные нейроны спинного мозга, ствола головного мозга или моторной коры (рис. 8). Это приводит к разрушению нейронов и последующему вялому параличу мышц: человек уже не может ими управлять, и мышцы со временем атрофируются. Как правило, под полиомиелитом (polios — «серый», myelos — «спинной мозг») понимают только паралитическую форму заболевания.
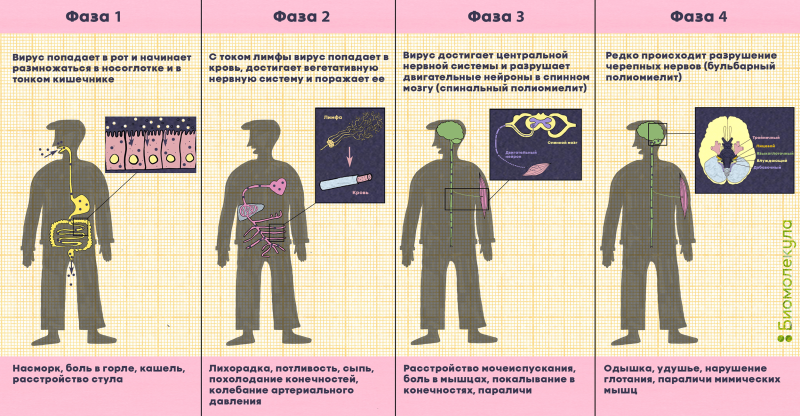
Рисунок 8. Развитие полиомиелита и симптомы заболевания. Полиовирус проникает в организм через рот и размножается в клетках желудочно-кишечного тракта, миндалинах и лимфатических узлах. С кровью и лимфой может достигать ЦНС и атаковать двигательные нейроны, расположенные в передних рогах спинного мозга и черепно-мозговых нервах (клетки в стволе головного мозга, подкорковых ядрах мозжечка, клетки в двигательных областях коры головного мозга).), вызывая паралич. При бульбарном полиомиелите могут повреждаться очень важные нервы: языкоглоточный (управляет глотанием и движениями языка), блуждающий (посылает сигналы к сердцу, кишечнику и легким), вспомогательный (управляет движениями шеи). Разрушение тройничного и лицевого нервов (полиомиелит Понтина) может вызвать проблемы со зрением и трудности с жеванием. При поражении диафрагмального нерва возникает паралич диафрагмы.
иллюстрация Ирины Ефремовой
На ранней стадии (сразу после окончания инкубационного периода) паралитический полиомиелит проявляется в виде лихорадки, головной боли, скованности спины и шеи, слабости и мышечных болей. У больных могут возникать затруднения при глотании и мочеиспускании, запоры, иногда наблюдается выпадение поверхностных и глубоких рефлексов (например, мышечные сокращения мышц руки или ноги при ударе ими по сухожилиям). Паралич обычно развивается через 1–10 дней после появления первых симптомов и прогрессирует в течение 2–3 дней.
Паралитические формы полиомиелита обычно делят на спинальные и бульбарные. Спинальный полиомиелит характеризуется поражением двигательных нейронов в спинном мозге, которые отвечают за движение мышц, включая туловище, конечности и межреберные мышцы. Бульбарный полиомиелит встречается реже (2% всех случаев паралитического полиомиелита). Это происходит, когда полиовирус проникает в черепно-мозговые нервы в бульбарной области ствола головного мозга (часть, которая соединяет кору головного мозга со спинным мозгом). Разрушение этих нервов ослабляет соответствующие мышцы, вызывая проблемы с дыханием, речью и глотанием. Если вирус разрушает нервные клетки, управляющие мышцами диафрагмы, больной перестает дышать самостоятельно, таких больных подключают к искусственному дыханию. Распространенным осложнением бульбарного полиомиелита является энцефалит, воспаление головного мозга.
Примерно в 19% всех случаев паралитического полиомиелита заболевание поражает нервы как спинного, так и головного мозга. Эта смешанная форма заболевания называется бульбарно-спинномозговым полиомиелитом. При этом часто поражаются верхний отдел шейного отдела спинного мозга, нервы, обеспечивающие глотание, и диафрагмальный нерв. Помимо затрудненного дыхания, при бульбарно-спинальной форме могут наблюдаться параличи конечностей и проблемы с сердцем.
Паралич, вызванный полиомиелитом, может привести к летальному исходу, если повреждены нервы, важные для жизненно важных функций (таких как дыхание). Каждые 2-20 человек из 100, у которых развивается паралич, умирают. Наиболее частой причиной смерти является отказ мышц диафрагмы (рис. 9а). Следовательно, наиболее опасны бульбарная и бульбарно-спинальная формы полиомиелита.
Какой паралич возникнет у больного и насколько он будет тяжелым, зависит от степени поражения нервной системы вирусом. Полный паралич возникает, когда погибает не менее четверти нервных клеток в спинном мозге. Паралич после полиомиелита обычно остается на всю жизнь. Частичное или полное восстановление двигательной активности возможно, но для этого требуется длительная реабилитация, при которой здоровые мышцы постепенно возьмут на себя работу парализованных (рис. 9б).
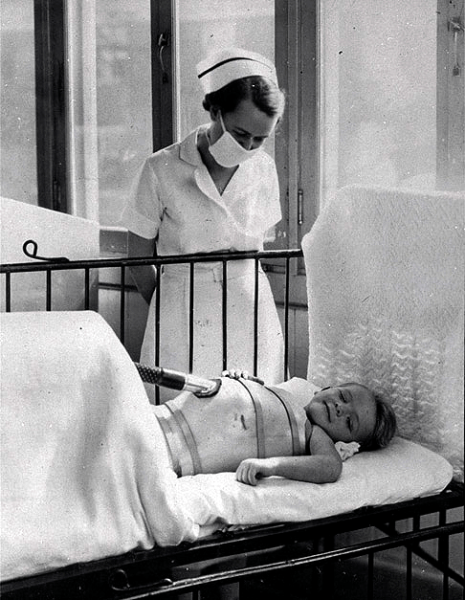
Рисунок 9а. Последствия полиомиелита: больной больницы Гордон Джексон, подключенный к портативному аппарату искусственной вентиляции легких, чтобы облегчить дыхание (1937, Торонто). Большинство смертей от полиомиелита вызвано разрушением нервов, отвечающих за дыхание.
Полиомиелит

Рисунок 9б. Последствия полиомиелита: выжившие после полиомиелита за обедом. Чаще всего парализующая форма заболевания заканчивается параличом руки или ноги.
«История кошмара детства — полиомиелита»
Никогда нельзя сказать заранее, будет ли инфицированный ребенок или взрослый парализован. Это всегда игра в рулетку. Однако недоедание, иммунодефицит, физические упражнения, хронические заболевания и повреждение скелетных мышц связаны с повышенным риском паралича из-за полиомиелита. Беременные женщины также восприимчивы к полиомиелиту. Они имеют более высокий риск как инфекции, так и осложнений [9].
Вероятность развития паралитического полиомиелита увеличивается с возрастом, как и степень паралича. У детей полиовирусное поражение центральной нервной системы чаще всего приводит к непаралитическому менингиту, при этом паралич возникает в одном случае из 1000. При этом чаще всего ограничивается поражением одной из ножек. У подростков и взрослых параличи вследствие полиомиелита возникают гораздо чаще, в одном из 75 случаев, и чаще носят обширный характер, распространяясь на грудь, живот и конечности.
Имеет значение и серотип возбудителя. Самые высокие показатели параличей (1 на 200 инфицированных) связаны с полиовирусом 1-го типа, а самые низкие (1 на 2000) — со 2-м типом [10]. Вирус 3 типа вызывает паралич в 1 из 1150 случаев. К сожалению, единственный циркулирующий дикий полиовирус 1 серотипа является наиболее опасным.
Помимо параличей, острый полиомиелит грозит различными осложнениями, в том числе пневмонией, сниженным расширением легких (ателектаз), воспалением сердечной мышцы (миокардит), а при бульбарной форме — острым расширением желудка, желудочно-кишечными расстройствами, язвами и кишечной непроходимостью [11]. Жертвы полиомиелита могут долгие годы страдать из-за поражения опорно-двигательного аппарата: сколиоза, защемления нервов и патологий сухожилий в спине. Даже после полного выздоровления, через 15–40 лет, инфекция может спровоцировать новые осложнения: повышенную утомляемость, боли, проблемы с дыханием, мышечную слабость и потерю работоспособности. Постполиомиелитный синдром встречается у 25% людей, перенесших паралитическую форму заболевания.
Полиомиелит и Фрида Кало
Фрида Кало, пожалуй, самая известная мексиканская художница. Ее слабое здоровье сыграло важную роль в творческом развитии Фриды (рис. 10).

Рисунок 10а. Фрида Кало и полиомиелит: автопортрет Фриды Кало, 1931 год. На рисунке, который был нарисован во время четырехлетнего пребывания художницы в Соединенных Штатах, изображена перевязанная язва желудка на ее правой ноге.

Рисунок 10б. Фрида Кало и полиомиелит: Подсолнухи — Диего Ривера, 1943 Работа Диего Риверы, мужа Фриды Кало, оказалась пророческой: на полотне маленький мальчик с лицом Диего Риверы грустно рассматривает куклу с оторванной правой ногой. Фрида Кало лишилась ноги 10 лет спустя.

Рисунок 10с. Фрида Кало и полиомиелит: Фрида Кало работает в постели, 1952 год. После аварии 1925 года, когда автобус с юной Фридой врезался в трамвай, художница всю жизнь страдала от травм и осложнений, проводя много времени в постели или в постели инвалидная коляска.
Еще до того, как она попала в аварию (автобус, в котором она ехала, столкнулась с трамваем), перевернувшую всю ее жизнь, Фрида Кало переболела полиомиелитом. В возрасте 6 лет он стоил ей нескольких месяцев в постели и больной ноги. Правая нога Фриды на протяжении всей жизни оставалась слегка деформированной. Она была короче левой, поэтому художнику пришлось использовать обувь с разной толщиной подошвы. В детстве артистка подвергалась нападкам со стороны сверстников из-за физического недостатка, и это оказало значительное влияние на и без того впечатлительного ребенка.
Со временем проблемы с ногой обострились, у Фриды даже начали появляться трофические язвы. Скорее всего, причиной этого, помимо полиомиелита, стали врожденные неврологические патологии.
Впоследствии Фрида Кало перенесла несколько операций на травмированной ноге, которые в итоге закончились гангреной и ампутацией ноги ниже колена в 1953 году, незадолго до ее смерти [12].
Диагностика и лечение
Полиомиелит диагностируется по наличию вирусной РНК в мазке из горла или кала. Кроме того, выявить инфекцию может помочь анализ крови на антитела, специфичные к полиовирусу. Обнаружение вируса в спинномозговой жидкости является явным, но не обязательным признаком паралитического полиомиелита.
Если полиовирус выделен от больного параличом, врачи дополнительно выясняют, дикий это вирус или вакцинный (да, вакцинный вирус очень редко может вызвать настоящее заболевание). Определение источника вируса важно, поскольку на каждый зарегистрированный случай паралитического полиомиелита, вызванного диким полиовирусом, приходится до нескольких тысяч бессимптомных носителей. Каждый случай заражения диким вирусом — это угроза эпидемии.
Эффективного лечения полиомиелита не существует. Все, что врачи могут сделать для уже инфицированного пациента, — это облегчить симптомы и снизить риск осложнений. Чтобы избежать развития вторичных инфекций в ослабленном организме, применяют антибиотики, в противном случае поддерживающая терапия включает обезболивающие, физические упражнения, массаж и полноценное питание. Иногда используются хирургические методы лечения, такие как удлинение сухожилий и пересадка нервов.
Борьба с полиомиелитом
Полиомиелит стал приобретать характер эпидемий в конце 19 — начале 20 вв., когда активно развивалась медицина и повышался уровень жизни в городах. Внимание к личной и общественной гигиене в то время способствовало снижению распространения энтеровирусов, в том числе полиовируса, среди детей раннего возраста, и все больше детей лишались естественно приобретенного иммунитета к инфекционным агентам. В то же время со снижением детской и старческой смертности во многих странах росло население, и быстро увеличивалось число молодых людей, подверженных риску заболевания полиомиелитом. В то же время сама болезнь и пути передачи были еще до конца не ясны, бороться с полиомиелитом было трудно, и он стал настоящим бедствием: от него умерли тысячи детей, а десятки тысяч стали инвалидами. В начале 1950-х годов вспышки полиомиелита в США ежегодно вызывали около 15 000 случаев паралича при населении чуть более 150 млн. В 1952 г там был зарегистрирован пик заболеваемости — 57 000 случаев и 21 000 паралитических больных [13].
Не было эффективных методов лечения, которых сейчас нет. Больные дети попадали в больницу, где проводили месяцы, а иногда и годы. В редких случаях последствия паралича смягчались длительной реабилитацией, но большинство детей оставались частично или полностью парализованными на всю оставшуюся жизнь. Если вирус поражал мышцы диафрагмы, больных помещали в металлические боксы, где работе легких помогало попеременное изменение давления внутри. Такие устройства называют «железными легкими».
Железные легкие
В истории борьбы с полиомиелитом важную роль играют аппараты, поддерживающие дыхание тяжелобольных. Они не всегда были такими, как сейчас. В середине прошлого века пострадавших от полиовируса спасали так называемые «резервуарные» аппараты ИВЛ (рис. 11), в которые полностью помещали человека. Суть их работы заключалась в изменении давления внутри аппарата, что заставляло воздух попеременно наполнять и выпускать легкие.

Рисунок 11а. «Железные легкие»: танковый вентилятор. Жертве полиомиелита такая машина может понадобиться на недели или годы, а иногда и на всю жизнь.
«Железные легкие — защита органов дыхания для пострадавших от полиомиелита»
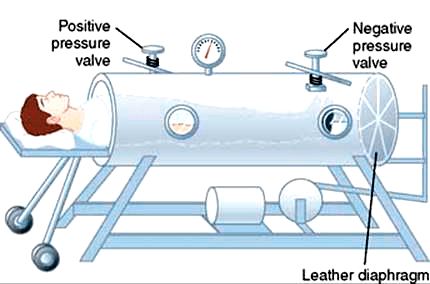
Рисунок 11б. «Железные легкие»: принцип работы устройства. Внутри камеры двигатель создает отрицательное давление, которое нагнетает воздух в легкие.
Дыхательная недостаточность — Патофизиология, диагностика, оксигенотерапия
Существовало множество модификаций «железных легких», заполнявших целые отделения в больницах (рис. 12).

Рис. 12. Больничная палата Бостона во время эпидемии полиомиелита 1955 г
«Последние из железных легких”»
очевидно, заключенным в «танках» пришлось нелегко. Они не могли оставить их без подключения к другому дыхательному аппарату, им приходилось все время лежать на спине и принимать жидкую пищу через зонды. Устройство может выключиться из-за сбоя питания. Но самое главное, применение «железных легких» не могло вылечить больных. Дети, пораженные вирусом, росли, жили и умирали, прикованные к металлической конструкции. Через год, проведенный в аппарате, пациенты уже не могут вернуться к нормальной жизни из-за атрофии дыхательной мускулатуры. Подключить таких пациентов к современному электростимулятору уже невозможно: их мышцы настолько слабы, что не могут функционировать даже с помощью искусственной стимуляции.
Сегодня обладателей «железных легких» очень мало. Прожив всю жизнь в аппарате, они постоянно находятся в страхе, опасаясь его обрушения. Часто сами пациенты или их родственники год за годом заняты поиском новых деталей для устаревших конструкций устройств. Например, Марта Лиллард, одна из немногих, кто все еще использует большую капсулу в 2020 году, собрала ее из двух машин, одна из которых обошлась ей в 8000 долларов. При кратковременном выходе женщины из «железных легких» ее дыхание поддерживается переносным аппаратом искусственной вентиляции легких (рис. 13).

Рисунок 13. Марта Лиллард рядом с железными легкими. Фото Дженнингса Брауна.
«Последние из железных легких”»
Профилактика полиомиелита включала изоляцию больных, дезинфекцию помещений и частое мытье рук. Все эти меры малоэффективны из-за большого количества бессимптомных носителей вируса, которых трудно выявить. Популярность получили и более необычные подходы. Например, в 1930-х годах в США были предприняты попытки остановить вспышки полиомиелита с помощью интраназального введения раствора сульфата цинка для прижигания слизистой оболочки. Метод был основан на ошибочном предположении, что полиовирус попадает в нервную систему через обонятельный нерв [14].
В 1921 г будущий президент США Франклин Рузвельт стал жертвой полиомиелита (рис. 14). Во многом из-за этого резко изменилось общественное мнение о полиомиелите: его перестали считать исключительно детской инфекцией. Позже, в 1938 году, Рузвельт основал Национальный фонд детского паралича для поддержки научных исследований и помощи тем, кто пострадал от этого заболевания. Вскоре фонд перерос в некоммерческую благотворительную организацию March of Dimes — «Марш десятицентовиков», — которая собирала пожертвования (рис. 15). Каждый цент был важен.

Рисунок 14. Президент США Франклин Рузвельт в инвалидном кресле. Он заболел полиомиелитом в возрасте 39 лет.
Инвалидное кресло Рузвельта

Рисунок 15а. В США разработка полиовирусных вакцин финансировалась благотворительным фондом March of Dimes, созданным Ф. Рузвельтом. На фото афиша, рекламирующая благотворительный бал в честь дня рождения президента. Текст плаката: «Атака на полиомиелит. Мы снова можем танцевать».
Википедия

Рисунок 15б. Плакат Марша Даймов, в ходе которого собирались средства на борьбу с полиомиелитом в США во время вспышки, 1940-е годы. Надпись на плакате: «Ваши центы помогли мне выздороветь». Пожертвования в 10 центов, отправленные народом Америки Белому дому в 1938 г., составили более 85 тыс долл. Общая сумма, собранная Фондом и направленная на борьбу с полиомиелитом в 1938-1955 гг., превысила 233 млн долл.
[восемь]
Благодаря усилиям March of Dimes (фонд, финансируемый исследованием вакцины) в середине 1950-х эпидемия в Соединенных Штатах была обращена вспять: Джонас Солк разработал первую инактивированную вакцину против полиомиелита.
Сегодня, в эпоху победы над полиомиелитом, целью организации является сохранение здоровья детей, а основные усилия направлены на профилактику преждевременных родов, основной причины детской смертности в мире с 2005 года.
Глобальная инициатива по борьбе с полиомиелитом
Крупные вспышки полиомиелита в середине 20-го века были настолько серьезными, что побудили страны создать Глобальную инициативу по ликвидации полиомиелита (ГИЛП) в 1988 г. (видео 1). Сегодня в этот альянс входят правительства 200 стран, которым помогают пять партнеров: Всемирная организация здравоохранения (ВОЗ), Ротари-клуб, Центры США по контролю и профилактике заболеваний (CDC), Детский фонд ЮНИСЕФ, Фонд Билла и Мелинды Гейтс, и Альянс ГАВИ по вакцинам и иммунизации.
Международные усилия по борьбе с распространением полиовируса привели к снижению заболеваемости паралитическим полиомиелитом на 99%. Считается, что эта инициатива помогла спасти около 16 миллионов человек, которые могли стать инвалидами, и 1,5 миллиона человек, которые могли умереть. Текущая цель инициативы — полностью искоренить полиомиелит. Одним из важнейших направлений работы является дальнейшая иммунизация населения против полиомиелита в эндемичных странах и регионах, где риск завоза полиовируса очень высок.
Видео 1. Глобальные усилия по борьбе с полиомиелитом. За прошедшие годы в рамках Глобальной инициативы по ликвидации полиомиелита было вакцинировано более 1,4 миллиарда детей. Это стало возможным благодаря слаженной работе миллионов волонтеров со всего мира. Инвестиции, направленные на борьбу с инфекцией, превышают 3 миллиарда долларов.
Одна болезнь, две вакцины
Сегодня всем ясно, что победа над полиомиелитом была бы невозможна, если бы не были разработаны вакцины против полиомиелита. Первой такой вакциной стала инактивированная формалином вакцина Джонаса Солка (ИПВ – инактивированная полиомиелитная вакцина) на основе дикого полиовируса. Его начали широко применять в США в 1955 году. Вирус для вакцины выращивали на ткани почек обезьян. ИПВ была эффективна, но имела очевидные недостатки: низкую эффективность, высокую стоимость и необходимость многократных инъекций для достижения результата. Производство вакцины Солка не было безопасным, вирусы из лаборатории могли кого-то заразить или даже попасть в вакцину, если был нарушен процесс инактивации .
Именно это произошло в США, когда вакцина только начинала производиться. Препарат Cutter Laboratories, содержащий живой дикий полиовирус, был введен 200 000 детей. В результате у 204 детей развился паралич, умерло 10 человек [15].
Кроме того, ИПВ провоцировала недостаточную выработку местного иммунитета в кишечнике. В результате привитые дети хотя и не болели, но все же оставались носителями инфекции. Тем не менее вакцина Солка помогла снизить заболеваемость полиомиелитом в несколько раз.
Важным достижением в ликвидации полиомиелита стала разработка живой пероральной полиомиелитной вакцины (ОПВ) после ИПВ. Получить живую вакцину было гораздо сложнее, чем инактивированную. Для этого нужно было ослабить все три типа дикого вируса, а затем доказать эффективность и безопасность полученного препарата. Изучение вакцины проводили на приматах, вводя вакцину в головной и спинной мозг животных. При этом нельзя было точно судить, как поведет себя будущая вакцина при использовании на людях.
Подробнее о том, как получают живые аттенуированные (аттенуированные) вакцины, читайте в одной из предыдущих статей нашего спецпроекта — «Разработка вакцин: как и чем моделировать заболевание?» [16]. — Эд.
Основой ОПВ были аттенуированные штаммы полиомиелита LS-c 2ab/KP2 (тип 1), P712 Ch 2ab/KP2 (тип 2) и Leon 12a1b/KP3 (тип 3), полученные американским вирусологом Альбертом Сабином в 1956 г. [17]. Помимо него над живой вакциной для Ледерле работали польские и американские вирусологи Хилари Копровски и Джеральд Кокс. Они ослабили вирусы, введя их в мозг хлопковых крыс. Копровский получил вакцину раньше Сабина и даже раньше Солка в 1950 году. Он испытал ее в Бельгийском Конго и в Польше, но она так и не получила признания в США [18].
На самом деле первые попытки создания живой вакцины против полиомиелита начались гораздо раньше [19], а в 1930-е годы идея вакцины против полиомиелита была практически похоронена из-за провальных экспериментов Джона Колмера, испытавшего опасный прототип живой вакцины вакцина у 10000-летнего ребенка. Подробнее об этом читайте в статье «История вакцинации» [20] в нашем спецпроекте. — Эд.
Альберт Сабин аттенуировал вирус в культурах тканей почек макак-резусов, после чего отобрал штаммы вируса, подходящие для вакцины. Они не могли вызвать заболевание, но провоцировали иммунный ответ организма, защищая его от диких полиовирусов в будущем.
Полиовирус типа 1 до появления вакцины вызывал примерно 80% всех паралитических случаев заболевания, поэтому при разработке ему уделялось повышенное внимание. Для создания вакцинного штамма типа 1 Сэбин использовал высоковирулентный штамм Mahoney, который был ослаблен повторным пересевом в культурах клеток почек и коже обезьяны. Аттенуированный штамм Sabin 2 типа был получен из дикого штамма P712, а вирус коровьей оспы 3 типа был получен из дикого штамма Leon [21].
Российские вирусологи сыграли важную роль в создании и внедрении ОПВ.
Отечественные ученые, победившие полиомиелит
Первые эпидемии полиомиелита в Прибалтике, Казахстане и Сибири начались в 1949 г., а в 1950 г в СССР было зарегистрировано более 17 тыс случаев заболевания [22]. В 1957 г., после поездки в Америку советских вирусологов — Михаила Петровича Чумакова, Марины Константиновны Ворошиловой (супруги М.П. Чумакова) и Анатолия Александровича Смородинцева (рис. 16), в СССР начали производить инактивированную вакцину Солка, но для борьбы было недостаточно быть больным. Требовался более эффективный, дешевый и удобный в использовании препарат. Этого можно было добиться за короткое время, используя ослабленные штаммы вируса, уже созданные Сэбином.

Рисунок 16а. Советские вирусологи, наладившие первое в СССР массовое производство живой оральной полиомиелитной вакцины: Михаил Петрович Чумаков (1909–1993) за работой. Российский вирусолог, внесший вклад в борьбу с клещевым энцефалитом, полиомиелитом и многими другими инфекционными заболеваниями. В 1950 году он возглавил Ивановский институт вирусологии, впоследствии переименованный в Институт полиомиелита и вирусных энцефалитов СССР. Разработана и внедрена живая оральная полиомиелитная вакцина на основе аттенуированных штаммов Альберта Сабина. Эта вакцина используется в 60 странах мира.
«Михаил Петрович Чумаков — советский вирусолог»
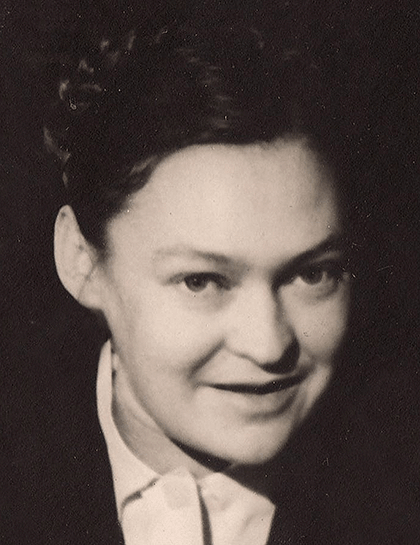
Рисунок 16б. Советские вирусологи, наладившие первое в СССР массовое производство живой оральной полиомиелитной вакцины: Марина Константиновна Ворошилова (1922–1986). Известный советский вирусолог. В 1958 г совместно с М.П.Чумаковым работал над внедрением живой вакцины против полиомиелита. Затем она разработала серию живых энтеровирусных вакцин для неспецифической защиты от вирусов гриппа, исследовала возможность использования энтеровирусов в качестве противораковых препаратов.
«Ворошилова Марина Константиновна (1922-1986)»

Рисунок 16с. Советские вирусологи, наладившие первое в СССР массовое производство живой оральной полиомиелитной вакцины: Анатолий Александрович Смородинцев (1901–1986) в лаборатории. Российский бактериолог, иммунолог, вирусолог. Основатель и первый директор НИИ гриппа им. Смородинцева Минздрава России. В 1960-х разработал отечественную вакцину против кори, получив ослабленный штамм вируса кори Ленинград-16. Работал над вакцинами против полиомиелита, гриппа, эпидемического паротита и клещевого энцефалита.
«Смородинцев Анатолий Александрович»
Осенью 1956 года Анатолий Смородинцев получил живые аттенуированные вирусы от Альберта Сабина, после чего в Институте экспериментальной медицины АМН СССР и в Институте полиомиелита и вирусных энцефалитов СССР (ныне Федеральный научный центр Научно-исследовательские разработки иммунобиологических препаратов им. М.П. Чумакова РАН), которые возглавил Михаил Чумаков, приступили к испытаниям живой вакцины. Ученые испытали препарат сначала на себе, потом на своих родственниках, ведь вакцина предназначалась для детей. Первым маленьким пациентом, получившим вакцину, стал пятилетний внук Смородинцева.
Анатолий Александрович Смородинцев решился: сделал прививку любимому внуку. Во имя здоровья миллионов детей это сделал человек, который лучше всех представлял себе последствия возможной неудачи. Это был подвиг во имя миллионов людей.
А.Б. Прутко «Прирученный вирус»
Чтобы доказать безвредность вакцинных вирусов человеческого происхождения, команда Смородинцева провела их передачу от человека к человеку. Новые поколения вируса были выделены из кишечника вакцинированных, выращены в культуре клеток и повторно введены в качестве вакцины. В результате был продемонстрирован высокий уровень безопасности препарата.
В 1958 году они успешно провели клинические испытания новой оральной вакцины и доказали ее эффективность. В 1959 г были проведены крупные испытания живой вакцины в Литовской и Эстонской ССР, где заболеваемость полиомиелитом была очень высока [21]. С января по май вакциной Сэбина было привито около 10 млн детей в 11 союзных республиках [23].
Результаты превзошли все ожидания — новых случаев заражения фиксировалось все меньше, а вакцинация в стране получила широкое распространение. В 1960 г в СССР было вакцинировано 72 млн человек. Вакцину было легко вводить, она не требовала инъекций и была намного дешевле, чем ИПВ. Благодаря отечественным исследователям полиомиелит в стране удалось остановить за 1,5 года [24].
После этой победы другие страны стали импортировать советскую вакцину. За весь период работы в Институте полиомиелита произведено около 6 миллиардов доз ОПВ. За научную разработку, организацию массового производства и внедрение в медицинскую практику живой полиомиелитной вакцины М.П. Чумаков и А.А. Смородинцев были удостоены Ленинской премии в 1963 г. США [25]. Задержка с внедрением живой вакцины в Америке была связана, в том числе, с недоверием американского научного сообщества к российским ученым и их методам оценки безопасности вакцины.
ИПВ и ОПВ сегодня
В настоящее время для профилактики полиомиелита используются как живые пероральные, так и инактивированные вакцины, вводимые подкожно или внутримышечно. Для лучшей защиты ВОЗ рекомендует как минимум три дозы (рис. 17) и последующую ревакцинацию. К сожалению, пока не все дети получают 3 дозы вакцины.
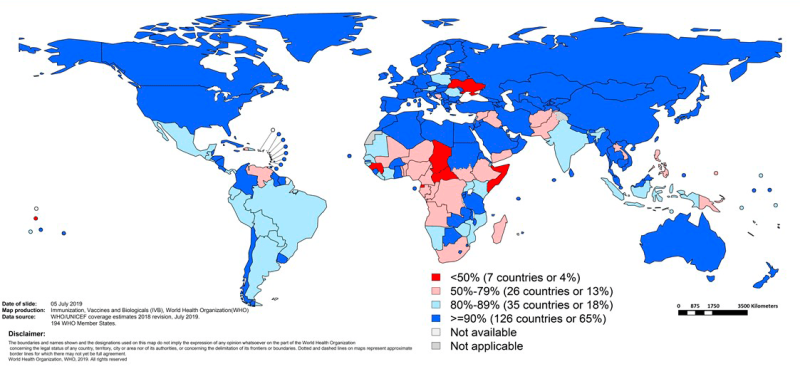
Рисунок 17. Доля детей, вакцинированных тремя дозами полиомиелитной вакцины во всем мире в 2018 г. Красным отмечены регионы, в которых уровень детской вакцинации против полиомиелита составляет менее 50% (Украина, Сомали, Чад, Центральноафриканская Республика, Экваториальная Гвинея, Гвинея).
ЧЬЯ
В мире используется пять типов вакцин против полиомиелита, в том числе:
- инактивированная вакцина против полиомиелита (ИПВ) против трех серотипов полиовируса;
- бивалентная оральная полиомиелитная вакцина (защищает от полиовирусов типов 1 и 3);
- моновалентные пероральные вакцины (защищают от определенных типов полиовируса 1 или 3).
Их широкое применение позволило добиться больших успехов в ликвидации паралитического полиомиелита (рис. 18).
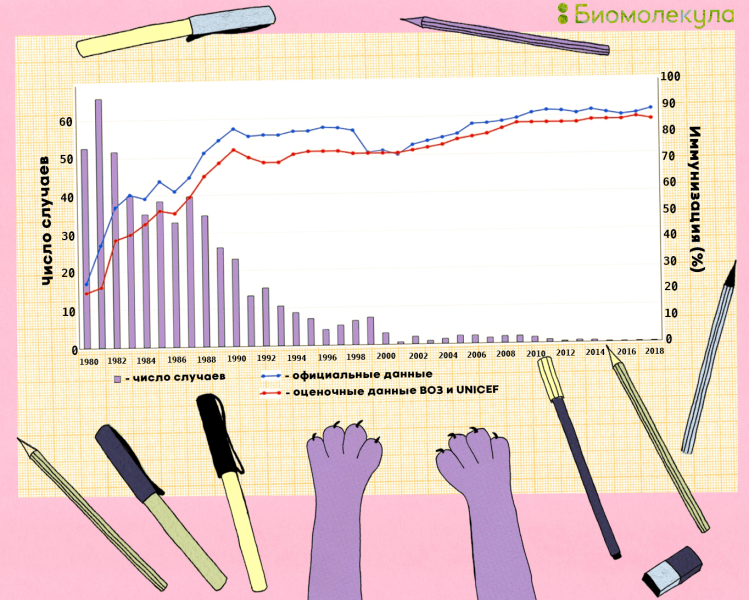
Рисунок 18. Число зарегистрированных случаев полиомиелита и распространение вакцины по всему миру, 1980–2018 гг. Синим цветом показаны официальные данные о количестве людей, вакцинированных тремя дозами вакцины против полиомиелита, красным цветом показаны оценки ВОЗ и ЮНИСЕФ.
иллюстрация Ирины Ефремовой по версии ВОЗ
Инактивированная трехкомпонентная вакцина (ИПВ)
ИПВ, созданная в 1955 году Солком, была значительно усовершенствована. Если раньше эффективность не превышала 80%, то сейчас она близка к 100% (после двух доз — около 89%) [26], [27], а иммунитет сохраняется пожизненно. Вакцина по-прежнему не вызывает интенсивного местного иммунного ответа в слизистой оболочке кишечника, поэтому вакцинированные только ИПВ часто продолжают элиминировать вирус с калом [28], но подавляют размножение вируса в носоглотке [29], [30][.]. Это означает, что ИПВ способна ограничивать распространение инфекции в регионах, где основной способ передачи вируса – воздушно-капельный.
В основе ИПВ обычно лежат дикие полиовирусы Mahoney (тип 1), MEF-1 (тип 2) и Saukett (тип 3), которые выращивают в культуре клеток Vero или диплоидных клеток человека, после чего их инактивируют формальдегидом. При производстве ИПВ строго контролируется концентрация каждого типа вируса – от этого зависит эффективность вакцины. ИПВ может быть самостоятельным препаратом или входить в состав многокомпонентных вакцин [31].
Инактивированную вакцину против полиомиелита вводят внутримышечно или подкожно. Она признана более безопасной, чем ОПВ, так как не несет ни малейшего риска развития вакциноассоциированного паралитического полиомиелита. Известные побочные эффекты после введения ИПВ включают покраснение (0,5–1%), уплотнение (3–11%) и болезненность (14–29%) в месте инъекции.
Основным недостатком ИПВ, несмотря на строгий производственный контроль, остается риск введения в вакцину живого дикого вируса. Некоторые страны, такие как Япония и Китай, уже лицензировали ИПВ на основе аттенуированных штаммов Сэбина [32], [33]. Такие препараты потенциально могут производиться в регионах, где заводы не могут обеспечить безопасное производство традиционной ИПВ.
Интересным способом получения полностью безопасной ИПВ может быть производство пустых вирусных капсидов, несущих все антигены вируса, но не вирусную РНК [34]. Это станет возможным, если такие «пустые» вирусы удастся стабилизировать и производить в больших количествах.
В то же время специалисты продолжают разрабатывать новые подходы к достижению ИПВ, которые помогут снизить затраты и повысить иммуногенность. Такие исследования включают процессы культивирования вирусов [35], методы введения вакцин [36] и использование новых адъювантов [37], [38].
Живые оральные полиовакцины
Современные живые оральные полиовакцины (ОПВ) содержат аттенуированные штаммы Сэбина типов 1, 2 и 3, прошедшие дополнительные пассажи и выращенные на первичных клетках почек африканской зеленой мартышки [39].
Эффективность ОПВ приближается к 100% после введения трех доз вакцины и зависит от выбранной схемы вакцинации, состава вакцины (считается, что трехкомпонентная ОПВ, от которой отказались в 2016 г., оказалась менее эффективной, чем двухкомпонентная) вакцина [40]) и условия проживания в регионе, где проводится иммунизация. Дети с недостаточным питанием с большей вероятностью останутся незащищенными даже после трех доз ОПВ [41], [42]. Эта проблема касается преимущественно бедных регионов и решается введением бустерных доз ИПВ [43]. Иммунитет против заболевания после вакцинации стойкий и, вероятно, сохраняется на всю жизнь [44].
Важным преимуществом живых вакцин является формирование местного иммунного ответа в кишечнике, что делает невозможным размножение дикого полиовируса в организме привитых детей. ОПВ также эффективны против полиомиелита в регионах с низким уровнем иммунизации. Вакцинный вирус может передаваться от привитого ребенка непривитому ребенку через грязные игрушки и посуду, а также защищает их. Привитый ребенок выделяет вакцинный вирус в окружающую среду в течение нескольких недель [45].
ОПВ, как и другие живые вакцины, влияет на врожденный иммунитет. В последние годы все большее количество исследований подтверждает неспецифический защитный эффект после вакцинации ОПВ, снижающий смертность от всех причин [46]. Это свойство живой вакцины может стать аргументом против отказа от нее в будущем.
Основным осложнением после ОПВ признан вакциноассоциированный полиомиелит (ВАПП), который неотличим от дикой инфекции.
ВАПП и ВРПВ и как с ними бороться
Оральные вакцины против полиомиелита (ОПВ) содержат ослабленный, но все еще живой вирус полиомиелита. К сожалению, в очень редких случаях (3-4 случая на 1 миллион вновь привитых ОПВ) вирус ОПВ может вызывать вакциноассоциированный паралитический полиомиелит (ВАПП) у детей, неотличимый от настоящего. Обычно это происходит при начале вакцинации сразу ОПВ и в 40% случаев вызывается вирусом 2 типа, входящим в состав вакцины. Часто осложнение связано с наличием у ребенка иммунодефицита или серьезных хронических заболеваний. ВАПП также может возникать у невакцинированных детей, которые были в контакте с ребенком, получившим ОПВ.
В Российской Федерации с 1998 по 2014 гг зарегистрировано 127 случаев ВАПП [47].
Для снижения риска ВАПП в большинстве стран, в том числе и в России, первую вакцинацию от полиомиелита делают детям с ИПВ (в России первые две), и только потом включают ОПВ. Эта тактика рекомендована ВОЗ для всех без исключения стран с 2016 г. Она давно зарекомендовала себя, например, в США (рис. 19) [48].
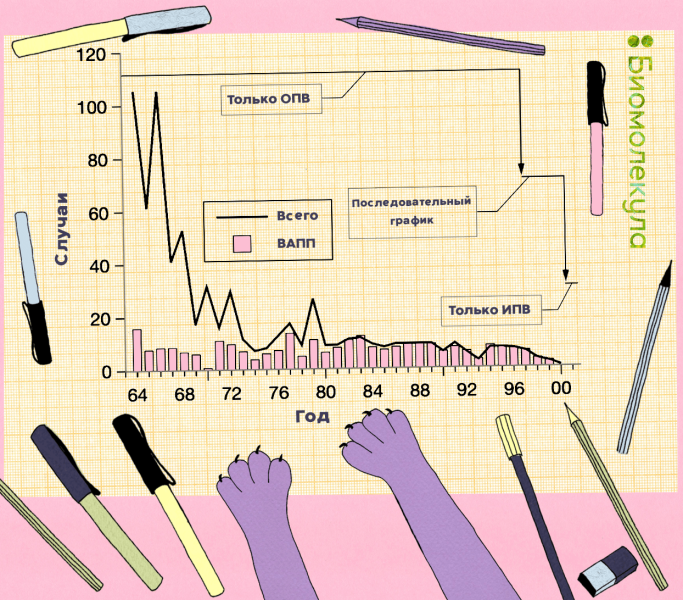
Рисунок 19. Общее количество случаев полиомиелита и случаев ВАПП, зарегистрированных в США, 1964–2000 гг. Внедрение последовательного плана ИПВ/ОПВ привело к снижению числа случаев ВАПП в стране.
иллюстрация Ирины Ефремовой по [60]
В России введение в 2008 г последовательной вакцинации ИПВ и ОПВ (2 дозы ИПВ + 1 доза ОПВ с последующей ревакцинацией ОПВ) позволило снизить число случаев ВАПП в 2,6 раза [47].
Еще одним эффективным способом является отделение детей, которые еще не получили первую дозу ИПВ, от тех, кто уже получил ОПВ. Официальные правила разделения детей до и после получения оральной вакцины в России предполагают еще более строгие меры (общение привитых ОПВ разрешается только после трех доз вакцины), но они, по мнению специалистов, весьма противоречивы и трудновыполнимы, учитывая необходимость посещения детьми детского сада.
Наконец, для снижения числа случаев ВАПП, вызванных вакцинным вирусом 2-го типа, с 2016 г не используется тройная ОПВ (дикий полиовирус 2-го типа больше не нуждается в защите, он был объявлен полностью ликвидированным в 2015 г.). Но ВАПП — не единственная причина отказа от трехвалентной живой вакцины.
Другая проблема связана с полиовирусами, связанными с вакцинами, или ПВВП.
Когда ОПВ вводят ребенку, вакцинный вирус не вызывает заболевания, а, как это было бы, размножается в миндалинах и кишечнике ребенка и попадает в кровоток, вызывает защитный иммунный ответ, а затем покидает организм.
При репродукции, когда вирус делает множество копий самого себя, часто происходят мутации, и в окружающую среду попадают уже мало измененные вакцинные штаммы, вакцинородственные полиовирусы (ВРПВ) (видео 2). Некоторые ПВВП снова могут быть опасны для человека и вызывать настоящий полиомиелит. В настоящее время в мире циркулируют все три типа ПВВП, но вирус типа 2 является причиной большинства случаев ВАПП.
Видео 2. Вакцинородственные полиовирусы (ВРПВ). Оральные вакцины против полиомиелита содержат ослабленные штаммы полиовируса, которые могут передаваться от вакцинированного человека другим людям, вызывая иммунный ответ и тем самым защищая их от полиомиелита. Очень редко эти вирусы восстанавливают нейровирулентность — способность вызывать паралитическую форму заболевания.
Вакцинный вирус легко передается от человека к человеку в районах, где много непривитых людей. Поэтому в основном там наблюдаются случаи ВАПП. Чем дольше живут ПВВП, тем больше мутаций они накапливают и тем выше риск того, что они вновь обретут вирулентность (могут вызвать заболевание).
Еще одной причиной возникновения ПВВП является длительное размножение вакцинного вируса в организме при ослабленном иммунитете. Если иммунная система не в состоянии справиться с вирусом ОПВ в течение обычных 8-11 недель, он может жить в организме очень долго и постепенно мутировать, становясь опасным (такие ПВВП называют иммунодефицитными).
Следует понимать, что ВРПВ — очень редкое явление. Дикий полиовирус наносит несравненно больший ущерб. За последние 10 лет и 10 миллиардов доз ОПВ было зарегистрировано 1000 случаев полиомиелита, вызванного циркулирующим ПВВП. Если бы ОПВ было прекращено, примерно 6,5 миллиона детей заразились бы обычным полиомиелитом за тот же период. ПВВП, ассоциированные с иммунодефицитом, вызывают полиомиелит еще реже: с 1962 г известно всего 111 случаев [49].
борьба со вспышками полиомиелита, вызванными циркулирующим ПВВП, ничем не отличается от стратегии борьбы с диким полиомиелитом, предусматривающей усиление эпиднадзора и широкомасштабную иммунизацию детей в возрасте до пяти лет. Это помогает остановить передачу вируса людям без специфического иммунитета (например, вспышка ВАПП в Сирии была остановлена в 2017 г. [50]). Как только дикий полиовирус будет ликвидирован, пероральные вакцины станут единственным источником живого полиовируса, и мир будет постепенно полностью отказываться от ОПВ, чтобы исключить риск новых случаев.
Несмотря на проблемы с ВАПП и ПВВП, важно понимать, что обе вакцины против полиомиелита, ОПВ и ИПВ, необходимы для полной ликвидации инфекции. ИПВ зарекомендовала себя как превосходная вакцина для высоко иммунизированных сообществ, а ОПВ – в условиях, где передача дикого вируса все еще сохраняется (таблица 1).
Новые стабильные вакцины
Ученые, стремясь снизить риск появления опасных штаммов вакцинных вирусов, продолжают работу над повышением их генетической стабильности. Разработка новых живых вакцин уже ведется в нескольких крупных институтах США и Великобритании. Первые испытания двух препаратов-кандидатов от полиовируса типа 2, финансируемые Фондом Билла и Мелинды Гейтс, прошли в Бельгии в 2017 г. (рис. 20). В исследовании приняли участие 30 человек.

Рис. 20. Полиополис — временное общежитие на 20 мест, построенное в Университете Антверпена (Бельгия) для проведения клинических испытаний новых живых полиомиелитных вакцин S2/cre5/S15domV/rec1/hifi3 и S2/S15domV/CpG40. Период пребывания в Полиополисе составил примерно 30 дней, в течение которых вирус продолжал обнаруживаться в фекалиях испытуемых.
Добро пожаловать в Полиополис: клиническое испытание nOPV2
Подход, используемый исследователями для получения генетически стабильных штаммов, основан на изменении некодирующего участка IRES вирусной РНК [51]. Другие методы улучшения стабильности полиовируса включают повышение точности репликации полимеразы и деоптимизацию кодирующих единиц в вирусной РНК [52], [53]. Пока еще рано судить о безопасности новых ОПВ, так как осложнения после ОПВ редки, а значит, исследования новых вакцин должны быть очень масштабными.
Таблица 1. Пероральные и инактивированные вакцины: в чем разница. Источник: Глобальная инициатива по ликвидации полиомиелита
| Оральная вакцина против полиомиелита — ОПВ | Инактивированная вакцина против полиомиелита — ИПВ | |
|---|---|---|
| Что входит в состав вакцины | Смесь живых аттенуированных штаммов полиовируса:
| Смесь убитых штаммов трех типов дикого (или ослабленного) полиовируса. |
| Как действует вакцина | Формируется как общий, так и местный иммунитет, препятствующий размножению дикого полиовируса в кишечнике и передаче от человека к человеку. Вакцинный вирус может передаваться от человека к человеку, увеличивая число иммунизированных людей в условиях нехватки вакцин. | Местный иммунитет на слизистых оболочках кишечника и носоглотки недостаточен для дальнейшего предотвращения размножения дикого вируса и его передачи другим людям. |
| Используемые функции | Поскольку вакцина вводится перорально, волонтеры могут помочь с ее распространением, что облегчит процесс иммунизации. ОПВ активно используется для борьбы как с диким вирусом, так и с ПВВП. Стоимость ОПВ составляет менее 0,15 доллара США за дозу. | Инъекции ИПВ должны проводиться только медицинскими работниками. Стоимость вакцины составляет 1 доллар США за дозу или более. |
| Риск ВАПП | 3-4 случая на 1 млн вновь привитых детей. ВАПП не может передаваться от человека к человеку и вызывать вспышки. | Абсолютно никакого риска. |
| Риск ПВВП | С 2000 года было использовано более 10 миллиардов доз ОПВ, в результате чего было зарегистрировано около 1000 случаев полиомиелита, связанного с ПВВП. | Абсолютно никакого риска. |
Графики вакцинации против полиомиелита
Схемы вакцинации против полиомиелита варьируются от страны к стране (рис. 21), при этом страны стараются соблюдать рекомендации ВОЗ, направленные на окончательную ликвидацию дикого полиовируса.
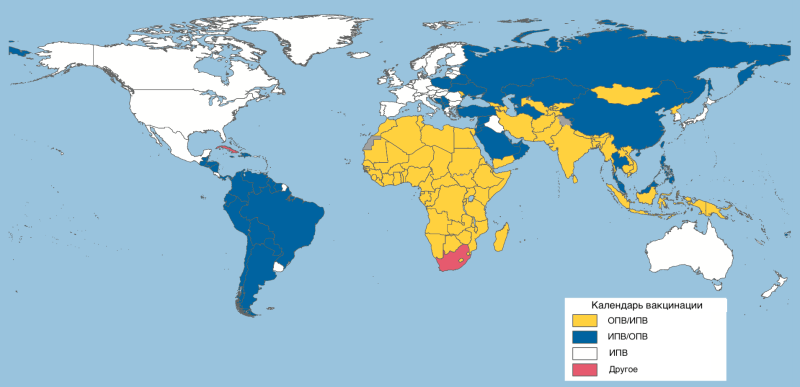
Рисунок 21. Планы вакцинации против полиомиелита в мире. Желтым цветом отмечены страны, в которых используется график, в котором ИПВ следует за ОПВ. Синим цветом отмечены страны, в которых планируется первичная вакцинация ИПВ с последующим введением доз ОПВ. Белый — страны, которые используют только ИПВ.
[60], рисунок адаптирован
Выбор вакцины против полиомиелита в той или иной стране зависит в основном от эпидемиологической ситуации и риска распространения дикого вируса, а также завоза вируса из эндемичных стран (рис. 22).
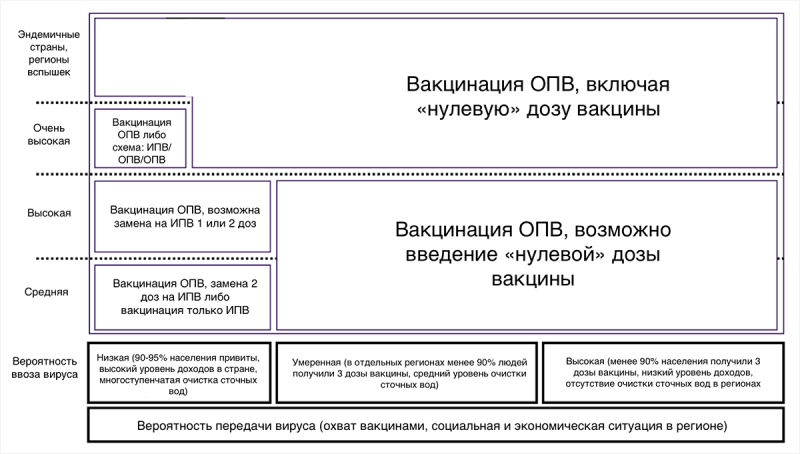
Рисунок 22. Рекомендации ВОЗ по выбору вакцин против полиомиелита в зависимости от риска распространения или завоза инфекции. Замена ОПВ на ИПВ рекомендуется только в странах с низкой вероятностью передачи дикого вируса (привито более 95% населения, высокий уровень гигиены в стране). Для эндемичных и опасных регионов также рекомендуется дополнительная «нулевая» доза ОПВ, которую вводят перед началом основного курса вакцинации, когда кишечник ребенка еще не заселен бактериями, способными снизить эффективность вакцины. Он усиливает иммунный ответ от последующих доз и не связан с повышенным риском ВАПП, поскольку в первые месяцы жизни младенец защищен материнскими антителами. ВОЗ подчеркивает необходимость обеспечения доступности вакцин для всех людей без исключения даже в регионах, свободных от полиомиелита.
«Вакцины против полиомиелита и иммунизация против полиомиелита в период, предшествующий искоренению: документ с изложением позиции ВОЗ», адаптированный рисунок
Во многих национальных календарях вакцинации (например, российских или китайских) ИПВ указывается как первая доза или первые две дозы. При этом вакцинацию начинают с двухмесячного возраста. Интервал между дозами ОПВ или ИПВ составляет 4–8 недель.
Взрослых обычно прививают только в том случае, если они входят в группу риска, а именно:
- отправиться в эндемичный/опасный район, где циркулирует вирус или существует высокий риск вспышек полиомиелита;
- работа в лаборатории с диким полиовирусом;
- являются медицинскими работниками и имеют дело с больными полиомиелитом.
Схема вакцинации взрослых групп риска включает 3 дозы ИПВ с интервалами 1–2 и 6–12 мес между дозами для тех, кто ранее не был вакцинирован, и 1 ревакцинацию для тех, кто получил весь курс вакцинации в детстве.
Вакцинация против полиомиелита в России
В России вакцинация против полиомиелита включена в Национальный календарь прививок и включает 6 доз вакцины (табл. 2).
Таблица 2. Вакцинация детей против полиомиелита в России.
| Доза | Вакцинация | Ревакцинация | ||||
|---|---|---|---|---|---|---|
| один | 2 | 3 | 4 | пять | 6 | |
| Возраст | три месяца | 4,5 месяца | 6 месяцев | 18 месяцев | 20 месяцев | 14 лет |
| Вакцина | ИПВ | ИПВ | дОПВ | дОПВ | дОПВ | дОПВ |
| dOPV представляет собой двухвалентную ОПВ, защищающую от 1-го и 3-го типов вируса. Для детей ВИЧ-позитивных матерей и детей в детских домах рекомендуется только ИПВ. | ||||||
ИПВ была выбрана в качестве первых двух доз на основании низкого риска завоза дикого полиовируса и высокого уровня охвата вакцинацией в стране. Вероятно, в ближайшие годы в России произойдет полная замена ОПВ на ИПВ, что устранит риск ВАПП и обеспечит высокий уровень защиты от всех серотипов полиовируса (установлено, что 3 дозы ИПВ защищают против вируса типа 2 лучше, чем 2 дозы [54]). Уже сейчас все дозы ОПВ могут быть заменены на ИПВ по желанию родителей, но не наоборот.
Прививка по эпидемическим показателям включает дополнительную дозу вакцины. Детей в этом случае вакцинируют ОПВ, если угрозу представляет дикий вирус, и ИПВ, если поводом для иммунизации является вакцинный вирус. Взрослых вакцинируют инактивированной вакциной.
Отечественный ИПВ Полимилекс производит ООО «Нанолек» (табл. 3). На сегодняшний день это единственная моноИПВ, широко доступная в стране. Он выпускается во флаконах, содержащих 5 доз препарата. Вскрытые флаконы пригодны для использования не более одних суток.
Центр исследований и разработок иммунобиологических препаратов. М.П. Чумакова Российской академии наук, проводятся клинические исследования новой инактивированной вакцины «ПолиовакСин» на основе штаммов Сэбина (с-ИПВ). Производство начнется в 2021 году. В планах центра также создание комбинированной вакцины с компонентом ИПВ, которая позволит делать одну инъекцию против нескольких инфекций одновременно.
Таблица 3. Вакцины против полиомиелита, зарегистрированные и используемые в Российской Федерации.
| Название вакцины | Режиссер | Компонент полиомиелита | Форма |
|---|---|---|---|
| Инактивированные вакцины, первые две дозы для вакцинации детей. Вакцинация взрослых | |||
| «Полимилекс» | ООО «Нанолек», Россия (производитель ООО «Нанолек», Bilthoven Biologicals, Нидерланды) | Инактивированные дикие вирусы типов 1, 2 и 3 | Суспензия для внутримышечного и подкожного введения |
| «Инфанрикс Гекса» (защищает от дифтерии, столбняка, коклюша, полиомиелита, гепатита В, гемофильной инфекции) | ООО «СмитКляйн Бичем-Биомед», Россия (производство Франция, Бельгия) | Суспензия для внутримышечного введения | |
| «Полиорикс» | ООО «СмитКляйн Бичем-Биомед», Россия (производство Франция, Бельгия) | Раствор для внутримышечных инъекций | |
| Имовакс Полио | Санофи Пастер С.А., Франция | Суспензия для внутримышечного и подкожного введения | |
| Пентаксим (защищает от дифтерии, столбняка, коклюша, полиомиелита, гепатита В) | Санофи Пастер С.А., Франция; ООО «Нанолек», Россия | Суспензия для внутримышечного введения | |
| «Тетраксим» (защищает от дифтерии, столбняка, коклюша, полиомиелита) | Санофи Пастер С.А., Франция | Суспензия для внутримышечного введения | |
| Живые вакцины, вакцинация и ревакцинация детей | |||
| «БиВак Полиомиелит» | ФГУП «ПИПВЭ им. М.П. Чумакова», Россия | Аттенуированные штаммы Сэбина 1 и 3 типов | Раствор для приема внутрь |
| «Моновак полиомиелит 2 тип» | ФГУП «ПИПВЭ им. М.П. Чумакова», Россия | Демпфированный ствол Sabin type 2 | Раствор для приема внутрь |
Вакцинация ИПВ противопоказана, если ранее была тяжелая реакция на вакцину или если у вас аллергия на антибиотики стрептомицин, неомицин или полимиксин В (они могут содержаться в вакцине в следовых количествах).
К противопоказаниям к ОПВ относятся: предшествующие негативные реакции на вакцину, иммунодефицитные состояния и наличие в окружающей среде детей раннего возраста, не вакцинированных против полиомиелита. Роспотребнадзор рекомендует невакцинированным детям избегать контакта с вакцинированными ОПВ в течение как минимум 60 дней после введения вакцины. Острое заболевание (или обострение хронического заболевания) является лишь временным противопоказанием к вакцинации. Плановые прививки можно делать через 2-4 недели после выздоровления или сразу после нормализации температуры при легких заболеваниях.
Что нужно сделать, чтобы полиомиелит исчез навсегда
Широкое использование вакцин против полиомиелита во всем мире привело к снижению глобальной заболеваемости полиомиелитом на 99% (рис. 23). Россия была объявлена свободной от полиомиелита в 1996 г. Последний случай полиомиелита, вызванного диким полиовирусом 2-го типа, произошел в Индии в 1999 г. Полиовирус 3-го типа не проявлялся с ноября 2012 г. Осталось победить только дикий вирус полиомиелита 1-го типа.
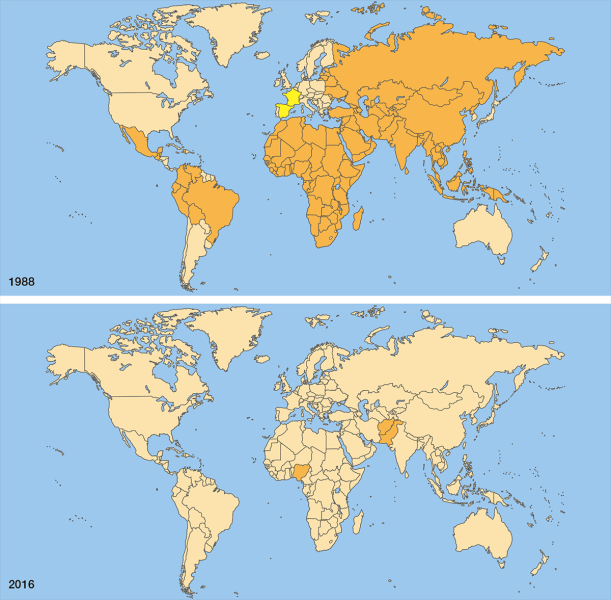
Рисунок 23. Полиомиелит до и после распространения вакцины. В 1988 г. (вверху) полиовирус циркулировал в 125 странах мира. На сегодняшний день (внизу) только Афганистан, Пакистан и Нигерия являются эндемичными по полиомиелиту (на карте отмечены оранжевым цветом, желтым отмечены страны с редкими завозными случаями полиомиелита).
[60]
Однако до тех пор, пока передача дикого вируса в эндемичных районах не будет полностью остановлена, риск новых вспышек заболевания будет сохраняться. Полиомиелит может в любой момент прийти из очага инфекции в страны, где болезнь давно побеждена, а иммунитет к вирусу у людей ослаблен или отсутствует, и тогда количество новых случаев вновь возрастет. В 2014 г в связи с распространением полиомиелита за пределы эндемичных регионов ВОЗ объявила чрезвычайную ситуацию в области общественного здравоохранения, требующую дополнительных рекомендаций по инфекционному контролю, которые остаются в силе.
На сайте ГИЛП есть онлайн-карта, на которой показаны все новые случаи. В 2019 г было зарегистрировано 176 случаев заражения диким полиовирусом (из них 29 в Афганистане и 145 в Пакистане) и 364 случая циркулирующим вакцинным вирусом (из них 129 случаев в Анголе). В России крупные вспышки полиомиелита произошли в 1995 г. (154 случая) и 2010 г. (14 случаев).
Пораженные полиомиелитом страны, где циркуляция дикого вируса еще не прервана, — это Пакистан, Афганистан и Нигерия. Там до сих пор происходит заражение из-за нехватки квалифицированного медицинского персонала, недоверия людей к вакцинам и бедности [55]. Экспертов больше всего беспокоит возможность передачи полиомиелита в другие страны из Афганистана и Пакистана (рис. 24).
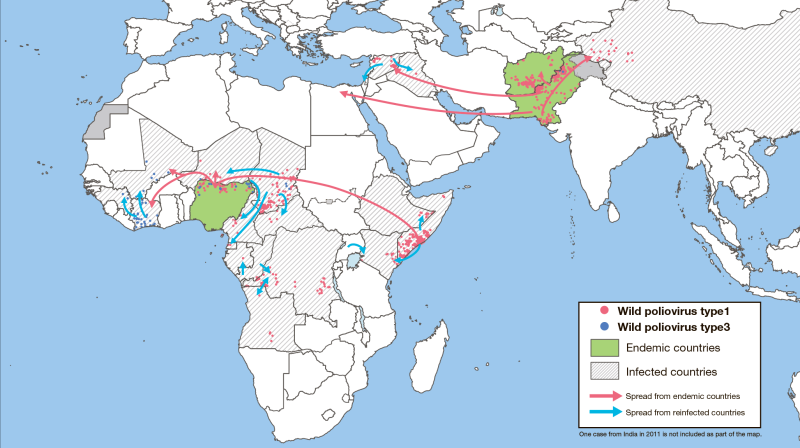
Рисунок 24. Случаи завоза дикого полиовируса из эндемичных и опасных районов, 2011–2014 гг. Красными стрелками показано, как дикий вирус мигрирует из эндемичных регионов Афганистана, Пакистана и Нигерии в другие страны. Синие стрелки показывают дальнейшее распространение вируса.
[60]
В ряде стран Африки (Ангола, Бенин, Буркина-Фасо, Республика Конго и др.), в Юго-Восточной Азии (Индонезия, Мьянма), в западно-тихоокеанском регионе (Китай, Малайзия, Филиппины) и в восточной части страна. Средиземноморье (Сомали) периодически возникает угроза новых вспышек заболевания из-за завоза дикого или циркулирующего вакциноассоциированного полиомиелита.
Поэтому вакцинация крайне важна для путешественников. Перед поездкой в страну, где существует риск контакта с полиовирусом, вы должны получить все необходимые дозы вакцины. Люди, которые не были вакцинированы более года, должны получить дополнительную ревакцинацию перед отъездом. Все путешественники из эндемичных стран должны быть должным образом вакцинированы и дополнительно получить дополнительную дозу живой или инактивированной полиомиелитной вакцины не менее чем за 4 недели (но не ранее, чем за 12 месяцев) до поездки для повышения защиты от инфекции и снижения возможности завоза полиовируса в полиомиелит. -свободные страны. В случае срочного отъезда сделать прививку все равно необходимо, даже не уложившись в сроки. Для людей, ранее вакцинированных одной ОПВ, ВОЗ рекомендует использовать живую полиомиелитную вакцину в качестве бустерной дозы [56].
Для получения дополнительной информации о прививках от полиомиелита для путешественников посетите веб-сайт ВОЗ в разделе «Международные путешествия и здоровье». — Эд.
Правительства стран, где риск передачи полиомиелита остается очень высоким, принимают специальные меры для защиты людей от инфекции. Например, при выезде за пределы Афганистана и Пакистана постоянные жители или туристы, находившиеся в опасной зоне более четырех недель, должны будут предъявить справку о предыдущей вакцинации. Некоторые страны, в том числе Египет, Индия, Марокко, Филиппины, Саудовская Аравия и Грузия, требуют при въезде от людей, прибывающих из стран, затронутых полиомиелитом, предъявить сертификат о прививках. Если сертификата нет, можно сделать прививку прямо на границе.
Болезнь можно победить, но для этого мы должны продолжать поддерживать программы вакцинации, разъясняя людям важность профилактики полиомиелита и проявляя гибкость в отношении вакцинации людей из всех социальных групп. Стратегия ВОЗ по ликвидации полиомиелита в настоящее время включает три этапа. Сначала это вытеснение диких вирусов вакцинными штаммами (вакцинация ОПВ), затем переход на ИПВ для исключения циркуляции вакцинородственных вирусов (ПВВП) и, наконец, постепенный отказ от вакцин в связи с отсутствием угрозы заражения. Сегодня этот план подвергается критике, а отказ от ОПВ активно обсуждается специалистами [57], [58]. Есть опасения, что полиомиелит вернется, обесценив долгие годы усилий врачей всего мира. Кроме того, ОПВ может играть значительную роль в снижении общей заболеваемости детей благодаря своему неспецифическому защитному эффекту. Многие видят решение этой проблемы в разработке новых и усовершенствованных вакцинных препаратов, обладающих всеми достоинствами ИПВ и ОПВ и лишенных их недостатков.
Об этом и многом другом нам рассказал Константин Чумаков, известный вирусолог, много лет работавший в Управлении по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) [59]. Как и его отец, Михаил Чумаков, он крупный специалист по полиомиелиту. — Эд.
Между тем победа над полиомиелитом близка как никогда, остается сделать последний шаг.
Литература
- Нора Эллен Гроус, Лена Морган Бэнкс, Майкл Эшли Стейн. (2014). Выжить после полиомиелита в постполиомиелитном мире. Социальные науки и медицина. 107, 171-178;
- Полиомиелит. В: Эпидемиология и профилактика вакциноуправляемых заболеваний (13-е издание). ЦКЗ, 2015 г;
- Ван-Шик Рю. (2017). Пикорнавирус. Молекулярная вирусология патогенных вирусов человека. 153-164;
- Дэвид Дж. Солеки, Матиас Громейер, Штеффен Мюллер, Гюнтер Бернхардт, Эккард Виммер. (2002). Экспрессия человеческого полиовирусного рецептора/гена CD155 активируется Sonic Hedgehog. Дж. Биол. Chem., 277, 25697-25702;
- Джонатан Р. Бауэрс, Джеймс М. Ридлер, Приянка Шарма, Кэтрин Джейда Экскоффон. (2017). Рецептор полиовируса: больше, чем просто исследование вирусного рецептора. 242, 1-6;
- Чумаков П.М., Морозова В.В., Бабкин И.В., Байков И.К., Нетесов С.В., Тикунова Н.В. (2012). Онколитические энтеровирусы. «Молекулярная биология». 5, 712-725;
- Тунг А.В. Педиатрия: учебник для студентов высших мед.уч.зав. IV уровня аккредитации. Винница: «Новая книга», 2010. – 839 с.;
- Что такое полиомиелит? (2019). CDC;
- Штеффен Мюллер, Эккард Виммер, Джеронимо Виолончель. (2005). Полиовирус и полиомиелит: рассказ о кишках, мозгах и случайном исследовании вируса. 111, 175-193;
- Н. Натансон, О.М. Кью. (2010). От возникновения до исчезновения: деконструкция эпидемиологии полиомиелита. Американский журнал эпидемиологии. 172, 1213-1229;
- Ишмухаметов АА, Синюгина АА, Чумаков КМ (2019). Разработка вакцинных препаратов для профилактики полиомиелита: современное состояние проблемы (обзор). «Современные технологии в медицине». 4, 200-215;
- Валмантас Будрис. (2013). Неврологический дефицит Фриды Кало и ее искусство. Успехи в исследованиях мозга. 241-254;
- Ханс ван Влит, Харри ван дер Авоорт, Марина Конин-ван Шпендонк. (2017). Полиомиелит, исторический. Международная энциклопедия общественного здравоохранения. 519-526;
- Э. В. ШУЛЬЦ. (1937). СУЛЬФАТ ЦИНКА ПРОФИЛАКТИКА ПРИ ПОЛИОМИЕЛИТЕ. ДЖАМА. 108, 2182;
- Оффит Пенсильвания (2006). Инцидент с Каттером: как первая в Америке вакцина против полиомиелита привела к растущему вакцинному кризису. JR соц. С. 99, 156;
- Разработка вакцины: как и как имитировать болезнь?;
- Консультативная группа по вакцинам против полиомиелита. (1985). ЧЬЯ;
- Фокс М. (2013). Хилари Копровски, разработавшая первую вакцину против полиомиелита с живым вирусом, умерла в возрасте 96 лет. The New York Times;
- Морис Броди, Элтон Голдблум. (1931). АКТИВНАЯ ИММУНИЗАЦИЯ ПРОТИВ ПОЛИОМИЕЛИТА У ОБЕЗЬЯН. Журнал экспериментальной медицины. 53, 885-893;
- История вакцинации;
- Лашкевич В.А. (2013). История создания в 1959 г. А. Сабином живой вакцины из ослабленных штаммов и идея ликвидации полиомиелита. «Проблемы вирусологии». 1, 4–10;
- АА Смородинцев. Разговоры о вирусах;
- Бенисон С. (1982). Международное медицинское сотрудничество: доктор Альберт Сабин, вакцина против живого полиомиелита и Советы. Вестник истории медицины. 56, 460-483;
- Шувалова Е.П., Белозеров Е.С., Беляева Т.В., Змушко Е.И. Инфекционные болезни. СПб: «Спецлит», 2015. – 727 с.;
- Анда Байкус. (2012). История вакцинации против полиомиелита. WJV. 1, 108;
- ЭММАНУЭЛЬ ВИДОР, КАРЛТОН МЕШЕВИЦ, СТЭНЛИ ПЛОТКИН. (1997). Пятнадцатилетний опыт работы с производимой Vero вакциной против полиовируса с повышенной силой действия. Журнал детских инфекционных заболеваний. 16, 312-322;
- CDC. (1988). Паралитический полиомиелит – Сенегал, 1986–1987 гг.: обновление исследования эффективности N-IPV. MMWR Морб. Смертельный. Еженедельно. Респ. 37, 257-259;
- Маджид Лаассри, Кэтлин Лоттенбах, Роберт Белше, Марк Вольф, Маргарет Реннелс и др. (2005). Влияние различных схем вакцинации на экскрецию штаммов пероральной полиовирусной вакцины. J ИНФЕКЦИОННЫЙ ДИС. 192, 2092-2098;
- Р. СЕЛЬВАКУМАР, т.д.ЖЕЙКОБДЖОН. (1987). Кишечный иммунитет, индуцированный инактивированной вакциной против полиомиелита вакцина. 5, 141-144;
- Х. Фаден, Дж. Ф. Модлин, М. Л. Томс, А. М. Макбин, М. Б. Фердон, П. Л. Огра. (1990). Сравнительная оценка иммунизации живыми аттенуированными и инактивированными трехвалентными полиовакцинами в детском возрасте: системные и местные иммунные реакции. Журнал инфекционных заболеваний. 162, 1291-1297;
- Карпова Е.В., Саркисян К.А., Мовсесянц А.А., Меркулов В.А. (2018). Вакцинация от полиомиелита на современном этапе. «Биопрепараты. Профилактика, диагностика, лечение. 4, 236-242;
- Хироюки Симидзу. (2016). Разработка и внедрение инактивированных вакцин против полиомиелита, полученных из штаммов Сэбина, в Японии вакцина. 34, 1975-1985;
- Че YC, Цзян Л, Шао CW (2010). Технико-экономическое обоснование использования иммунизации Сэбин-ИПВ в постликвидационную эпоху в Китае. Чжунго И Мяо Хе Миан И. 16, 72–75;
- Клодин Порта, Абхай Котеча, Элисон Берман, Терри Джексон, Цзиншан Рен и др. (2013). Рациональная разработка рекомбинантных капсидов пикорнавируса для производства безопасного защитного антигена вакцины. PLoS Патог. 9, е1003255;
- Барбара П. Сандерс, Дайана Эдо-Матас, Джером Х.В. Кастерс, Мартин Х. Колдейк, Винсент Кларен и др. (2013). Клетки PER.C6® в качестве бессывороточной суспензионной клеточной платформы для производства полиовируса с высоким титром: потенциальный недорогой вариант мировых поставок инактивированной полиовирусной вакцины вакцина. 31, 850-856;
- Соня Резик, Алина Техеда, Педро Мас Лаго, Мануэль Диас, Аня Карменатес и др. (2010). Рандомизированное контролируемое клиническое исследование дробных доз инактивированной полиовирусной вакцины, вводимой внутрикожно с помощью безыгольного устройства на Кубе. J ИНФЕКЦИОННЫЙ ДИС. 201, 1344-1352;
- Паулин Вердейк, Нинке Ю. Ротс, Моник Г.С.Т ван Ойен, М. Стивен Оберсте, Клэр Дж. Буг и др. (2013). Безопасность и иммуногенность инактивированной полиовирусной вакцины на основе штаммов Сэбина с гидроксидом алюминия и без него: исследование фазы I на здоровых взрослых вакцина. 31, 5531-5536;
- Сьюзан Л. Болдуин, Кристофер Б. Фокс, Марк А. Палланш, Рея Н. Колер, Стивен Дж. Рид, Мартин Фриде. (2011). Повышенная активность инактивированной трехвалентной полиомиелитной вакцины с эмульсиями масло-в-воде вакцина. 29, 644-649;
- Рекомендации по обеспечению качества, безопасности и эффективности живой ослабленной полиомиелитной вакцины (пероральной). (2012). ЧЬЯ;
- Роланд В. Саттер, т.д.жейкоб Джон, Хемант Джайн, Шарад Агархедкар, Падмасани Венкат Раманан и др. (2010). Иммуногенность двухвалентной оральной полиовакцины типов 1 и 3: рандомизированное двойное слепое контролируемое исследование. Ланцет. 376, 1682-1688;
- Джон Т. (1992). Вакцина против полиомиелита и борьба с полиомиелитом в Индии. Всемирная конференция по полиомиелиту и кори;
- П. А. Патриарка, П. Ф. Райт, т.д.ж. Джон. (1991). Факторы, влияющие на иммуногенность пероральной полиомиелитной вакцины в развивающихся странах: обзор. Клинические инфекционные заболевания. 13, 926-939;
- Консепсьон Ф. Эстиварис, Хамид Джафари, Роланд В. Саттер, т.д.жейкоб Джон, Вибхор Джайн и др. (2012). Иммуногенность бустерных доз вакцины против полиомиелита для детей в возрасте 6–9 месяцев в Морадабаде, Индия: рандомизированное контролируемое исследование на базе местных сообществ. Ланцет Инфекционные заболевания. 12, 128-135;
- Патрик В. Келли. (1991). Восприимчивость молодых взрослых американцев к вакциноуправляемым инфекциям. ДЖАМА. 266, 2724;
- M. BENYESH-MELNICK, JL MELNICK, WE RAWLS, I. WIMBERLY, J. BARRERA ORO, et al. (1967). ИССЛЕДОВАНИЯ ИММУНОГЕННОСТИ, КОММУНИКАЦИОННОСТИ И ГЕНЕТИЧЕСКОЙ СТАБИЛЬНОСТИ ОРАЛЬНОЙ ПОЛИОВАКЦИНЫ, ПРИМЕНЯЕМОЙ ЗИМОЙ1. Американский журнал эпидемиологии. 86, 112-136;
- Питер Оби, Кристин С. Бенн. (2020). Прекращение введения живых вакцин после ликвидации болезни может увеличить смертность вакцина. 38, 10-14;
- Иванова Ольга Евгеньевна, Еремеева Татьяна Петровна, Морозова Надежда Сергеевна, Шакарян Армен Константинович, Короткова Екатерина Алексеевна и др. (2018). Вакциноассоциированный паралитический полиомиелит в Российской Федерации в 1998–2014 гг. Международный журнал инфекционных заболеваний. 76, 64-69;
- Лоррейн Нино Александр. (2004). Изменения политики в отношении вакцин и эпидемиология полиомиелита в Соединенных Штатах. ДЖАМА. 292, 1696;
- Полиовирусы вакцинного происхождения. ПГЕИ;
- Отчет № 27 о ситуации со вспышкой цПВВП2 в Сирии. (2017). ЧЬЯ;
- Пьер Ван Дамм, Ильза Де Костер, Ананда С. Бандйопадхьяй, Хильде Реветс, Канчанамала Витанаге и др. (2019). Безопасность и иммуногенность двух новых живых аттенуированных моновалентных (серотип 2) пероральных полиовирусных вакцин у здоровых взрослых: одноцентровое двойное слепое исследование фазы 1. Ланцет. 394, 148-158;
- Эндрю Дж. Макадам, Джеральдин Фергюсон, Дэвид М. Стоун, Джанет Мередит, Сара Ноулсон и др. (2006). Рациональный дизайн генетически стабильных живых аттенуированных полиовирусных вакцин всех трех серотипов: актуальность для ликвидации полиомиелита. ОВИ. 80, 8653-8663;
- Филип ре минор. (2012). Программа ликвидации полиомиелита и финальные вопросы. Журнал общей вирусологии. 93, 457-474;
- С.М. Харит, В.С. Покровский, А.А. Рулева, И.В. Фридман. (2016). Программа ВОЗ по ликвидации полиомиелита: проблемы и решения. Педиатрическая фармакология. 13, 289-298;
- Обзор эндемичных по полиомиелиту стран. (2018). ЧЬЯ;
- Вакциноуправляемые заболевания и вакцины. ЧЬЯ;
- Константин Чумаков, Элли Эренфельд, Экард Уиммер, Вадим И. Агол. (2007). Вакцинацию против полиомиелита нельзя прекращать. Nat Rev Microbiol. 5, 952-958;
- В. Агол, Дж. Виолончель, К. Чумаков, Э. Эренфельд, Э. Виммер. (2016). Искоренение полиомиелита: поиск баланса. Наука. 351, 348-348;
- Константин Чумаков об эпидемии SARS-CoV-2, стратегии ликвидации полиомиелита и своих знаменитых родителях;
- Роланд В. Саттер, Олен М. Кью, Стивен Л. Кочи, Р. Брюс Эйлуорд. (2018). Живая вакцина против полиомиелита. Вакцины Плоткина. 866-917.e16.
[Источник]








